
Aufbau und Grundprinzipien der optischen Kohärenztomographie.
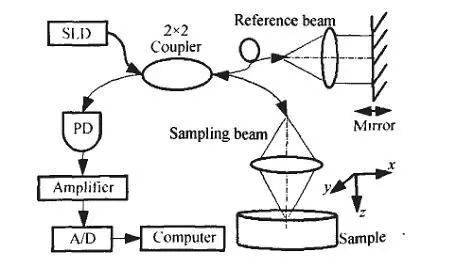
Optische Kohärenztomographiebasiert auf dem Prinzip des Interferometers, verwendet schwach kohärentes Nahinfrarotlicht, um das zu testende Gewebe zu bestrahlen, und erzeugt Interferenz basierend auf der Kohärenz des Lichts. Es verwendet Superheterodyne-Erkennungstechnologie, um die Intensität des reflektierten Lichts für die oberflächliche Gewebebildgebung zu messen. . Das OCT-System besteht aus einer niederkohärenten Lichtquelle, einem faseroptischen Michelson-Interferometer und einem photoelektrischen Detektionssystem.
Das Herzstück von OCT ist das Faser-Michelson-Interferometer. Das von der niedrigkohärenten Lichtquelle Superlumineszenzdiode (SLD) emittierte Licht wird in die Singlemode-Faser eingekoppelt und durch den 2×2-Faserkoppler in zwei Pfade aufgeteilt. Ein Weg ist das Referenzlicht, das von der Linse kollimiert und vom Planspiegel zurückgeworfen wird. ; Der andere ist der Abtaststrahl, der von der Linse auf die zu testende Probe fokussiert wird.
Auf dem Detektor verschmelzen das vom Reflektor zurückgeworfene Referenzlicht und das rückgestreute Licht der zu untersuchenden Probe. Wenn die optische Wegdifferenz zwischen den beiden innerhalb der Kohärenzlänge der Lichtquelle liegt, tritt eine Interferenz auf. Das Ausgangssignal des Detektors spiegelt die Rückstreuung des Mediums wieder. In Richtung Streuintensität.
Scannen Sie den Spiegel und zeichnen Sie seine räumliche Position auf, so dass das Referenzlicht mit dem rückgestreuten Licht aus verschiedenen Tiefen im Medium interferiert. Je nach Spiegelposition und entsprechender Interferenzsignalintensität erhält man die Messdaten unterschiedlicher Tiefen (z-Richtung) der Probe. Das Ergebnis wird dann in Kombination mit dem Abtasten des Probenstrahls in der x-y-Ebene vom Computer verarbeitet, um die dreidimensionale Strukturinformation der Probe zu erhalten.
Die Entwicklung der OCT-Bildgebungstechnologie
Mit der weit verbreiteten Anwendung von Ultraschall im Bereich der Augenheilkunde hofft man, ein Nachweisverfahren mit höherer Auflösung zu entwickeln. Das Aufkommen von Ultrasound Biomicroscope (UBM) erfüllt diese Anforderung bis zu einem gewissen Grad. Es kann eine hochauflösende Bildgebung des vorderen Segments durch die Verwendung von Schallwellen mit höherer Frequenz durchführen. Aufgrund der raschen Dämpfung hochfrequenter Schallwellen in biologischen Geweben ist deren Detektionstiefe jedoch bis zu einem gewissen Grad begrenzt. Wenn Lichtwellen anstelle von Schallwellen verwendet werden, können die Defekte kompensiert werden?
1987 haben Takada et al. entwickelte ein optisches Niedrigkohärenz-Interferometrie-Verfahren, das zu einem Verfahren zur hochauflösenden optischen Messung mit Unterstützung von Faseroptik und optoelektronischen Komponenten weiterentwickelt wurde; Youngquistet al. ein optisches kohärentes Reflektometer entwickelt, dessen Lichtquelle eine Superlicht emittierende Diode ist, die direkt mit einer optischen Faser gekoppelt ist. Ein Arm des Instruments, der einen Referenzspiegel enthält, befindet sich im Inneren, während die Glasfaser im anderen Arm mit einem kameraähnlichen Gerät verbunden ist. Diese haben die theoretische und technische Basis für die Entstehung von OCT gelegt.
1991 verwendete David Huang, ein chinesischer Wissenschaftler am MIT, das entwickelte OCT, um die isolierte Netzhaut und die Koronararterien zu vermessen. Da die OCT eine beispiellos hohe Auflösung hat, ähnlich der optischen Biopsie, wurde sie schnell für die Messung und Bildgebung von biologischem Gewebe entwickelt.
Aufgrund der optischen Eigenschaften des Auges entwickelt sich die OCT-Technologie in klinischen Anwendungen der Augenheilkunde am schnellsten. Vor 1995 verwendeten Wissenschaftler wie Huang OCT, um Gewebe wie Netzhaut, Hornhaut, Vorderkammer und Iris des menschlichen In-vitro- und In-vivo-Auges zu messen und abzubilden, wodurch die OCT-Technologie kontinuierlich verbessert wurde. Nach mehreren Jahren der Verbesserung wurde das OCT-System weiter verbessert und zu einem klinisch praktischen Erkennungswerkzeug entwickelt, zu einem kommerziellen Instrument gemacht und schließlich seine Überlegenheit in der Fundus- und Netzhautbildgebung bestätigt. OCT wurde 1995 offiziell in Augenkliniken eingesetzt.
1997 wurde OCT schrittweise in der Dermatologie, dem Verdauungstrakt, dem Harnsystem und kardiovaskulären Untersuchungen eingesetzt. Ösophagus-, Magen-Darm-, Harnsystem-OCT und kardiovaskuläre OCT sind allesamt invasive Untersuchungen, ähnlich wie Endoskope und Katheter, jedoch mit höherer Auflösung und zur Beobachtung von Ultrastrukturen. Die Haut-OCT ist eine Kontaktinspektion, und auch die Ultrastruktur kann beobachtet werden.
Das erste in der klinischen Praxis verwendete OCT ist OCT1, das aus einer Konsole und einer Leistungskonsole besteht. Die Konsole umfasst einen OCT-Computer, einen OCT-Monitor, ein Bedienfeld und einen Überwachungsbildschirm; Das Kraftwerk umfasst ein Fundusbeobachtungssystem und ein Interferenzlichtsteuerungssystem. Da die Konsole und die Leistungsplattform relativ unabhängige Geräte sind und die beiden durch Drähte verbunden sind, hat das Instrument ein größeres Volumen und einen größeren Raum.
Das Analyseprogramm von OCT1 gliedert sich in Bildverarbeitung und Bildvermessung. Bildverarbeitung umfasst Bildstandardisierung, Bildkalibrierung, Bildkalibrierung und -standardisierung, Bild-Gauß-Glättung, Bild-Median-Glättung; bildgebende Verfahren sind weniger, nur die Netzhautdickenmessung und die retinale Nervenfaserschichtdickenmessung. Da OCT1 jedoch über weniger Scanverfahren und Analyseverfahren verfügt, wurde es schnell durch OCT2 ersetzt.
OCT2 wird durch Software-Upgrade auf der Basis von OCT1 gebildet. Es gibt auch einige Instrumente, die die Konsole und den Leistungstisch zu einem OCT2-Instrument kombinieren. Dieses Instrument reduziert den Bildmonitor und beobachtet das OCT-Bild und überwacht die Scanposition des Patienten auf demselben Computerbildschirm, aber die Bedienung ist die gleiche wie bei OCT1. Ähnlich, es wird manuell über das Bedienfeld bedient.
Das Erscheinen von OCT3 im Jahr 2002 markierte eine neue Stufe der OCT-Technologie. Neben der benutzerfreundlicheren Bedienoberfläche von OCT3 können alle Operationen auf dem Computer mit der Maus durchgeführt werden, und seine Scan- und Analyseprogramme werden immer perfekter. Noch wichtiger ist, dass die Auflösung von OCT3 höher ist, seine axiale Auflösung beträgt 10 µm und seine laterale Auflösung 20 µm. Die Anzahl der von OCT3 erfassten axialen Proben hat sich im ursprünglichen 1-A-Scan von 128 auf 768 erhöht. Daher hat sich das Integral von OCT3 von 131.072 auf 786.432 erhöht, und die hierarchische Struktur des gescannten Gewebequerschnittsbildes ist klarer.
Copyright @ 2020 Shenzhen Box Optronics Technology Co., Ltd. – China Glasfasermodule, Hersteller von fasergekoppelten Lasern, Lieferanten von Laserkomponenten. Alle Rechte vorbehalten.